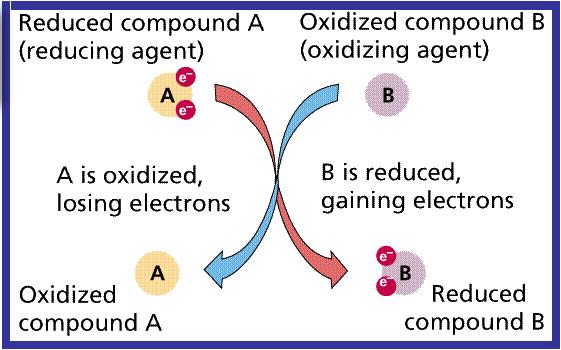
Redokspotentsiaal
Redokspotentsiaal ehk oksüdatsioonipotentsiaal on keemilise elemendi või ühendi tendents liita elektrone ja seetõttu redutseeruda. Igal elemendil/ühendil on temale omane redokspotentsiaal, kusjuures mida positiivsem ehk suurem on elemendi/ühendi redokspotentsiaal, seda kõrgem on tema afiinsus elektronide suhtes ehk võime redutseeruda. Redokspotentsiaali mõõdetakse tavaliselt millivoltides. Redokspotentsiaali standardväärtuseks loetakse kokkuleppeliselt standardvesinikelektroodi väärtust, mis võrdsustatakse väärtusega 0,00 mV. Seetõttu mingi ühendi redokspotentsiaal on suhteline väärtus – võrdlus standardvesinikelektroodiga. Nagu eelnevalt mainitud, näitab toidu redokspotentsiaal (Eh), kas toidul on tendents omandada elektrone e saada redutseeritud või loovutada elektrone e saada oksüdeeritud. Toidu redokspotentsiaal sõltub hapniku kontsentratsioonist keskkonnas ja selle toidule ligipääsemisest, näitks toidu tihedusest, sest see mõjutab otseselt hapniku läbimisvõimet. Toidu pH langusel ühe ühiku võrra tõuseb redokspotentsiaal +58 mV võrra.